Ocorrência de fungos e micotoxinas em grãos de milho em Jataí-GO, Brasil
Occurrence of fungi and mycotoxins in corn grains in Jataí – GO, Brazil.
DOI: http://dx.doi.org/10.23850/24220582.342
Juliana Teodora de Assis Reges*, Michelle Nogueira de Jesus, Simone Duarte Ramalho da Silva, Marcelo Henrique de Souza, Iago Jesus Santos, Samara Moreira do Santos e Josiane Walleria Rodrigues
1Universidade Estadual de Goiás- Campus de Jataí- GO (UEG), Brasil.
Autor correspondente: juliana.teodora@bol.com.br
Recibido: 23-08-2016 Aceptado: 29.10.2016
Para citar este artigo
Reges, J., Nogueira de Jesus, N., Duarte, S., Henrique de Souza, M., Santos, I., Moreira do Santos, S. & Walleria, J. (2016). Ocorrência de fungos e micotoxinas em grãos de milho em Jataí-GO, Brasil. Rev. Colomb. Investig. Agroindustriales, 3(1), 34-39. DOI:http://dx.doi.org/10.23850/24220582.342
RESUMO
O milho é um produto muito suscetível à contaminação por fungos muitas vezes, facilitada pelas condições de armazenagem dos grãos. Dessa forma, a qualidade sanitária das sementes pode ser comprometida devido ao ataque de patógenos que interferem em sua viabilidade. O trabalho teve como objetivo identificar, quantificar e avaliar a ocorrência de fungos, e verificar a incidência de micotoxinas (aflatoxina e zearalenona) em grãos de milho, na pós colheita. Foram coletadas 7 amostras de grãos de milho em propriedades na região do município de Jataí/GO. O experimento foi desenvolvido no laboratório da Universidade Estadual Goiás, Campus de Jataí- GO. O delineamento experimental utilizado foi em blocos ao acaso, por 7 tratamentos e cinco repetições. A etapa A da pesquisa foi a identificação de diferentes espécies fúngicas, foram analisadas as características macroscópicas e microscópicas. A etapa B do projeto foi a deteção de mitoxinas nos fungos encontrados. Em todas as amostras analisadas foram identificados os fungos Aspergillus flavus, Fusarium moniliforme, Fusarium roseum, e Penicillium sp. A presença do fungo aflatoxigênico e a produção de aflatoxinas foram encontradas em algumas amostras de grãos de milho que apresentaram níveis de contaminação acima do limite oficial (20 µg/ kg) permitido pelo Ministério da Saúde/Anvisa e o MAPA.
Palavras-chave: Aflatoxinas, colheita, semente de milho, zearalenona.
ABSTRACT
Corn is a product very susceptible to fungal contamination often facilitated by the grain storage conditions. Thus, the sanitary quality of seeds it may be compromised due to the attack of pathogens that interfere with their viability. The study aimed to identify, quantify and evaluate the occurrence of fungi, and check the incidence of mycotoxins (aflatoxin and zearalenone) in corn grain in post harvest. 7 were collected samples of corn grain in properties in the city of Jataí / GO region. The experiment was developed in the laboratory of Goiás State University, Campus of Jataí-GO. The experimental design was a randomized block for 7 treatments and five repetitions. Step A of the research was the identification of different fungal species, macroscopic and microscopic characteristics were analyzed. The B phase of the project was the mitoxinas detection in fungi found. In all samples the fungus were identified, Aspergillus flavus, Fusarium moniliforme, Fusarium roseum, e Penicillium sp. The presence of aflatoxigênico fungus and the production of aflatoxins were found in some samples of corn kernels that had contamination levels above the official limit (20 mg / kg) permitted by the Ministry of Health / ANVISA and MAPA.
Keyword: Aflatoxins, corn seed, crop, zearalenona.
INTRODUÇÃO
A produção agrícola bem como a indústria de alimentos sofrem perdas econômicas, oriundas de contaminações dos alimentos, no mundo inteiro. Os fatores que afetam o crescimento de fungos nos grãos de milho são principalmente teor de água dos grãos, temperatura, tempo, condição física (grãos quebrados) e sanitária do grão, nível de inóculo do fungo, conteúdo de oxigênio e armazenamento, insetos e ácaros (Pezzini et al., 2005).
Contudo, o crescimento do fungo e a presença de toxinas não são sinônimos, porque nem todos os fungos produzem toxinas. Os gêneros dos fungos mais comumente associados com toxinas que ocorrem, naturalmente, são Aspergillus, Penicillium e Fusarium (Iamanaka et al., 2010).
O milho é um substrato perfeito para contaminação fúngica, uma vez que o amido é o componente principal do grão. Segundo Farias et al., (2000), a contaminação por fungos com potencial toxigênicos, tais como Aspergillus sp., Fusarium sp. e Penicillium sp., pode ocorrer em grãos de milho aparentemente sadios.
Almeida et al., (2000) avaliaram a microbiota fúngica em amostras de três híbridos de milho recém-colhidos, provenientes de três regiões distintas do Estado de São Paulo. Os autores encontraram, em média, 71,1; 46,7 e 22,7% de incidência de Fusarium sp., Penicillium sp e Aspergillus sp., respectivamente, indicando a predominância destes três gêneros sobre outras espécies fúngicas, e concluíram que fatores abióticos, tais como o teor de umidade nos grãos de milho, a atividade de água, a precipitação pluvial e a temperatura do ar influenciam diretamente no nível de contaminação fúngica, bem como na potencialidade toxigênica das cepas de Aspergillus flavus e de Fusarium moniliforme quanto à produção de micotoxinas.
De acordo com Resolução da ANVISA RDC N°. 7 de 18 de fevereiro de 2011 existem cinco micotoxinas fúngicas que foram consideradas de maior risco à saúde humana e animal. Estas toxinas são: aflatoxinas (AFLA), ocratoxina A (OTA), zearalenona (ZON), desoxinivalenol (DON) e fumonisinas (FUMO).
Devido essas micotoxinas causarem danos à saúde humana, deve-se avaliar a qualidade de grãos que está disponível na nossa região verificando a adequação de armazenagem e a pós colheita. Machinski et al., (2001), avaliaram 110 amostras de milho recém-colhido no estado de São Paulo e encontraram 54,5% das amostras contaminadas com aflatoxina B1, com níveis variando de 6 a 1600 ppb. Ocratoxina A foi encontrada em 2 amostras (206 e 128 ppb) e zearalenona em uma amostra (4640 ppb).
As condições climáticas de um país determinam, em grande parte, as classes de fungos que irão crescer e os tipos de micotoxinas que podem produzir. No Brasil, existem condições propícias para o crescimento de todo tipo de fungos produtores de micotoxinas. Na pesquisa tem aparecido trabalhos que foram constatados a ocorrência de micotoxinas nos alimentos que são consumidos no Brasil, e a incidência de aflatoxinas e zearalenona em milho.
O trabalho teve como objetivo identificar, quantificar e avaliar a ocorrência de fungos, e verificar a incidência de micotoxinas (aflatoxina e zearalenona) em grãos de milho na pós colheita.
MATERIAL E MÉTODOS
Amostras
Neste trabalho foram coletadas 7 amostras de milho em 7 propriedades rurais, situadas na região de Jataí/GO no sudoeste goiano com a latitude: 17° 52’ 53” S, Longitude: 51° 42’ 52” W. As médias de temperatura foram 28 C° de máxima e mínima de 11 ° C, e umidade relativa do entre 20 e 40%, no mês de julho de 2015. Os períodos em que as coletas das amostras de milho foram realizadas, iniciou-se após a colheita de julho de 2015.
Para as análises das amostras de milho foram coletadas aproximadamente 1,0 Kg de grãos e foram acondicionadas em frascos plásticos codificados para identificação e quantificação de fungos e de micotoxinas (aflatoxinas e zearalenona). Para a identificação e quantificação dos fungos foram utilizados os grãos de milho inteiros e para as demais determinações as amostras foram moídas, classificadas por tamanho de partícula em peneira 20 mesh, submetidas ao quarteamento e analisadas em cinco repetições. O experimento foi desenvolvido no laboratório da Universidade Estadual Goiás, Campus de Jataí-GO.
Isolamento e Identificação Fúngica Nas amostras de grãos de milho foi utilizado o método adotado por Christensen e Meronuck (1986), modificado. Para o isolamento foram plaqueados 100 grãos por amostragem em cinco placas, em meio de cultura de BDA (ágar 15 g.L-1), Potato Dextrose (18,5 g.L-1), Estreptomicina (0,050 g.L-1) e Cloranfenicol (0,050 g.L-1) e ficou incubada em estufa a 25°C por 5 dias.
Foram plaqueadas 20 grãos em cada placa, de modo que fiquem dispostos em 4 fileiras de 5 grãos cada. Os grãos de milho ficaram com o germe ou embrião voltados para cima e para a mesma direção, afim de facilitar a leitura posterior.
A identificação e quantificação dos fungos foram realizadas com o auxílio de microscópio estereoscópico, onde se quantificou em percentual de crescimento, considerandose a presença ou ausência de contaminação em 100 grãos de milho. Outras análises foram determinadas para identificar a espécie fúngica sendo elas: características morfológicas, macroscópicas, cor, textura, pigmento difusível no meio de cultura, produção e característica dos exsudados, microscópicas e microestruturas (colônia). Os dados de quantificação dos fungos foram realizados estatisticamente pelo teste de Tukey (p<0,01). Utilizandose o programa SISVAR (Ferreira, 2011), sendo que o experimento foi replicado, e conduzido em duas partes, a primeira replica foi realizada entre os meses de setembro e novembro de 2015 e a segunda replica foi conduzida entre dezembro e fevereiro de 2016.
Deteção de Micotoxinas
A extração e purificação das aflatoxinas (B1, B2, G1 e G2) foi feita segundo Soares e Rodriguez-Amaya (1989). As aflatoxinas foram identificadas e quantificadas por cromatografia em camada delgada, devido o material utilizado nessa análise está disponível no laboratório (placas de sílica gel 60 G, Merck), utilizando-se como fase móvel tolueno:acetato de etila: clorofórmio:ácido fórmico (70:50:50:20 v/v/v/v), descrita por Gimeno (1999). As leituras das fluorescências de amostra e padrões foram feitas em densitômetro, a 366 nm e o cálculo das concentrações foi obtido através das curvas de calibração. A Curva das aflatoxinas (AF) foi realizada com os seguintes valores: AFB1 = 1,189 μg/mL; AFB2 = 0,91 μg/mL; AFG1 = 1,61 μg/mL e AFG2 = 1,39 μg/mL. Essas concentrações foram aplicadas nas quantidades de 1,0 ; 2,0 e 4,0 μL com cinco repetições.
A zearalenona foi extraída e quantificada segundo procedimentos descritos por Visconti e Pascale (1998). A quantificação foi realizada em cromatógrafo líquido de alta eficiência com detector de fluorescência (excitação λ = 267 nm e emissão λ = 450 nm), coluna Agilent Zorbax C18 (5 μm, 250 x 4,6 mm), pré-coluna Agilent Zorbax C18 (5 μm, 25 mm x 4,6 mm), com fluxo de 1 mL/minuto. A fase móvel foi composta por água ácida (3 % de ácido acético v/v): metanol (50:50, v/v) e injeção de 50 μL de amostra, descrita por Pezzini et al., (2005). A zearalenona foi quantificada utilizando para o cálculo, uma curva de calibração analítica. A curva da zearalenona foi feita com padrão contendo as concentrações de 1,5; 2,5; 5,0; 10,0 e 15,0 μL/mL. As amostras foram aplicadas para confecção da curva.
Os limites de detecção de aflatoxinas considerados foram de 1,0 μg/Kg (85,5 % de recuperação) e para a zearalenona de 10,0 μg /Kg (80 % de recuperação) (Pezzini et al., 2005).
RESULTADOS E DISCUSSÃO
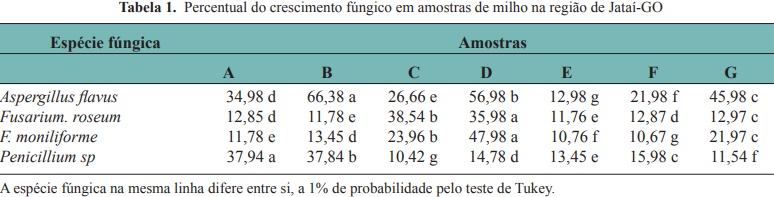
De acordo com os resultados do trabalho em relação ao crescimento fúngicos, encontraram as espécies Aspergillus flavus, Fusarium roseum, Fusaruium moniliforme e Penicillium sp, Todas espécies diferem estatisticamente (p<0,01). (Tabela 1).
O Aspergillus flavus apresentou variação de 12,98 a 66,38 % de crescimento em amostras milho após a colheita. Da mesma forma, os autores Pezzini et al., 2005 constataram diferentes resultados de percentagem do fungo Aspergillus flavus, variando de 38,71 a 76,85% em grãos de milho. Além disso, o patógeno pode ter sido favorecido pelas altas temperaturas (Iamanaka et al.,2010).
De acordo com os resultados o fungo Fusarium roseum nas amostras, variou de 11,78 a 38,54%. O Fusarium sp.é considerado um fungo de campo, que invade os grãos e sementes durante o amadurecimento e o dano é causado antes da colheita. Entretanto, não se desenvolvem durante o armazenamento, exceto ocasionalmente em grãos de milho armazenados com alto teor de umidade. (Pezzini et al., 2005).
Pode-se observar que o desenvolvimento do F. moniliforme em relação ao crescimento fúngicos, foram de 10,67 a 47,98% sementes retiradas no campo. Marcia e Lazzari (1998) encontraram 97,5 % das amostras de milho em grãos, 13,6 % das amostras de grits e 79 % das amostras de fubá infectadas por Fusarium, sendo a espécie predominante F. moniliforme. A espécies de Fusarium sp. estão causando uma série de doenças nas culturas em toda a parte do mundo gerando perdas econômicas significativa (Villa-Martínez et al., 2015).
De acordo com os resultados de desenvolvimento fúngicos do Penicillium sp. houve uma variação de percentagem de 10,42% a 37,94% das amostras milho coletadas no campo. Dos diferentes fatores que podem influenciar no crescimento destes fungos são as condições climáticas, pré-colheita, diferenças genéticas, índice de grãos quebrados, presença de insetos, entre outros (Bento et al., 2012). Segundo Farias et al., (2000), a contaminação por fungos com potencial toxigênicos, tais como Aspergillus sp., Fusarium sp. e Penicillium sp., pode ocorrer em grãos de milho aparentemente sadios.
Dilkin et al., (2000), verificaram contaminações fúngicas de 23,6; 57,1 e 14,3% de Aspergillus sp., Fusarium sp e Penicillium sp., respectivamente, em grãos de cinco híbridos de milho recém-colhidos, com 18% de umidade, em Santa Maria, Estado do Rio Grande do Sul. Kikuti et al., (2003), verificou-se em sementes de duas variedades de milho de polinização livre, na variedade AL 25, as contaminações foram de 44,8; 100; 0,67 e 0,33% com os fungos F. graminearum, Penicillium sp., Aspergillus niger e A. flavus, respectivamente. Na variedade BRS106, as percentagens de contaminação foram de 31,0 e 98,7% de Fusarium graminearum e de Penicillium sp., respectivamente.
Avaliando o efeito do retardamento da colheita de milho, constataram que a permanência prolongada das espigas de milho na planta, após a maturidade fisiológica, influenciou na redução da incidência de Fusarium moniliforme, seguindo a redução da umidade presente nos grãos. Por outro lado, os autores Santin et al., (2004), observaram que houve aumento da incidência de espécies dos gêneros Aspergillus e Penicillium, quando os grãos foram colhidos com umidades menores.
De acordo com os resultados das análises de aflatoxinas (B1, B2, G1 e G2), na tabela 2, podemos verificar que dentre as 7 amostras analisadas, 5 delas apresentaram níveis de toxidade de aflatoxinas. Uma explicação plausível para essa contaminação seria que diferentes fatores influenciaram o crescimento de fungos toxigênicos e a produção de aflatoxinas, sendo eles: a umidade relativa do ar, a temperatura e o teor de água presentes nos grãos (Dilkin et al., 2000).
Os níveis de contaminação variaram de 1 a 10 µg/kg de aflatoxina B1, de 1 a 12 µg/kg de aflatoxina B2, de 1 a 12 µg/kg de aflatoxina G1, aflatoxinas G2 e ZEA não foram detectadas.
De acordo com os resultados obtidos, podemos verificar que as amostras C, D e F ultrapassaram os limites oficial pela Anvisa para a soma B1+B2+G1+G2 sendo 27; 25; 22 µg/ kg respectivamente. De acordo pelo Ministério da Saúde/Anvisa e pelo Ministério da Agricultura, Pecuária e Abastecimento para alimentos destinados ao consumo humano, a somatória dos níveis de contaminação de (B1+B2+G1+G2) não pode ultrapassar de 20 µg/ kg. Esse limite é comparável aos estabelecidos por outros países e recomendado pela Organização para Alimentação e Agricultura.
No Brasil, outros trabalhos também relataram a ocorrência de aflatoxinas em milho e seus derivados, com percentagens de contaminação variando de 1,5% a 100% e níveis de 30 a 33 µg/kg. Esse fato foi constatado por Cortes et al.(2000), quando 28,57% das amostras de milho retiradas de lavouras do estado de Mato Grosso apresentavam nível médio de aflatoxinas de 12,35 µg/ kg, indicando que o milho no ponto de colheita já apresentava contaminação por aflatoxinas. Ramos et al. (2008), avaliaram a ocorrência natural das aflatoxinas (B1, B2, G1 e G2) em grãos de milho do estado de Goiás (Jataí, Montevidéu e Goiânia) e verificaram que os grãos já apresentavam aflatoxinas em níveis de 0 a 277,8 µg/kg de B1, de 0 a 14 µg/kg de B2, de 0 a 34,1 µg/kg de G1, e não foi detectada a aflatoxina G2.
Os autores Marques et al. (2009), analisaram a incidência de fungos dos gêneros Aspergillus, Fusarium e Penicillium e as contaminações com micotoxinas em grãos de cinco híbridos comerciais de milho em função da umidade de colheita, e observaram que a produção de aflatoxinas ocorreu em grãos ainda nas espigas, no campo, devido a condições ambientais favoráveis aos patógenos. A aflatoxina tem recebido grande atenção em comparação com as demais micotoxinas, devido aos efeitos carcinogênicos que pode provocar em animais e o efeito agudo tóxico em seres humanos. As aflatoxinas representam o grupo de micotoxinas com mais resultados positivos em alimentos já relatados (Pereira et al., 2002).Os trabalhos de ocorrência de fungos e micotoxinas em alimentos consumidos no Brasil, têm contribuído para avaliação e estudos das medidas a serem tomadas para prevenção de contaminação. Incidência de aflatoxinas em derivados de milho e zearalenona em milho, têm sido relatadas (Ramos et al.,2008; Pezzini et al., 2005; Pereira et al., 2002).
Recomenda-se para o milho, grau de umidade na colheita de 24 a 32 % e no armazenamento de 13 a 14 % (sem risco de deterioração por um ano) e de 12 % por um período superior a 1 ano (Pezzini et al., 2005). Os fungos necessitam de uma umidade relativa acima de 65 % o que corresponde a uma taxa de equilíbrio de umidade de 13 % no grão de cereal e eles crescem com temperaturas entre 10 e 40°C (Pezzini et al., 2005).
Medidas preventivas devem ser tomadas em todo o estágio de plantio, colheita, transporte, estocagem e processamento do produto final. Algumas medidas práticas como colher imediatamente o produto ao atingir a maturidade, secar o produto até níveis seguros de umidade, sementes oleaginosas e grãos deverão ser limpos para remover matéria orgânica, as áreas de armazenamento deverão ser limpas e livres de insetos e roedores, protegidas das influências climáticas (Iamanaka et al., 2010). Essas medidas podem contribuir para se não eliminar totalmente, pelo menos manter em níveis bem baixos e aceitáveis a presença de micotoxinas em alimentos destinados ao consumo humano e dos animais. Com relação a zearalenona podemos verificar que não houve níveis de contaminação nas 7 amostras analisadas. De acordo com os autores Oliveira et al. (2002), em produtos de derivados de milho, encontraram níveis de contaminação médio de zearalenona de 195,2 μg/ kg. Na maioria das pesquisas estudadas a zearalenona permanece em níveis mais baixos de 12,26 μg/kg (Pezzini et al., 2005).
Os resultados obtidos nesse trabalho foram importantes para identificar os níveis de contaminações fúngicas e micotoxinas encontradas nos grãos de milho analisados, pois a falta dessas informações acarretaria prejuízos à saúde dos consumidores.
CONCLUSõES
Os fungos A. flavus, F. moniliforme, F. roseum, e Penicillium sp, foram isolados e identificados, apresentando uma ampla faixa de variação no crescimento, de 12,98 a 66,38 %, de 11,78 a 47,98%, de 11,78 a 38,54 % e de 10,42 a 37,94 %, respectivamente. A presença do fungo aflatoxigênico e a produção de aflatoxinas ocorreram a partir da infeção dos grãos de milho em condições de campo. As amostras C, D e F de milho apresentaram níveis de contaminação acima do limite oficial (20 µg/kg) permitido pelo Ministério da Saúde/Anvisa e o MAPA.
AGRADECIMENTOS
À Universidade Estadual de Goiás (UEG), Campus de Jataí-GO pela concessão da aprovação do projeto.
REFERÊNCIAS
Almeida, A. P., Correa, B., & Mallozzi, M. A. B. (2000). Mycoflora and aflatoxin/fumonisin production by fungalisolates from freshly harvested corn hybrids. Braz J Microbiol, 31(4), 321-326. http://dx.doi.org/10.1590/ S1517-83822000000400016
Bento, L.F., Caneppele, M.A.B., Albuquerque, M.C.F., Kobayasti, L., Caneppele, C., & Andrade, P.J. (2012). Ocorrência de fungos e aflatoxinas em grãos de milho. Rev Inst Adolfo Lutz, 71(1),44-9.
Cortes, N.A., Cassetari-Neto, D., & Correa, B. (2000). Ocorrência de aflatoxinas em milho produzido pelo sistema tradicional de cultivo, em comunidades de agricultura familiar, no estado de Mato Grosso. Hig Alimentar, 14(77), 16-25.
Christensen, C.M., & Meronuck, R.A. (1986). Quality maintenance in stored grains and seeds. Minessota: University of MN Press (Eds.), p.150.
Dilkin P, Mallmann CA, Santurio JM, & Hickmannet J. L. (2000). Classificação macroscópica, identificação da microbiota fúngica e produção de aflatoxinas em híbridos de milho. Ciênc Rural, 30(1), 137-41. http://dx.doi.org/10.1590/S0103-84782000000100022
Farias, A. X., Robbs, C. F., Bittencourt, A. M., Andersen, P. M., & Corrêa, T. B. S. (2000). Contaminação endógena por Aspergillus sp. em milho pós-colheita no Estado do Paraná. Pesq Agropec Bras, 35 (3), 617-621. http://dx.doi.org/10.1590/S0100-204X2000000300018
Ferreira, D.F. (2011). Sisvar: a computer statistical analysis system. Ciênc Agrotec, 35(6), 1039-1042. http://dx.doi.org/10.1590/S1413-70542011000600001
Gimeno, A.(1979). Thin layer chromatographic determination of aflatoxins, ochratoxins, sterigmatoxystin, zearalenone, citrinin, T-2 toxin, diacetoxyscirpenol, penicillic acid, patulin and penitrem A. J Assoc Off Anal Chem, 62, 579-85.
Gimeno, A.(1979). Thin layer chromatographic determination of aflatoxins, ochratoxins, sterigmatoxystin, zearalenone, citrinin, T-2 toxin, diacetoxyscirpenol, penicillic acid, patulin and penitrem A. J Assoc Off Anal Chem, 62, 579-85.
Kikuti, A. L. P., Vasconcelos, R. C., Marincek, A., & Fonseca, A. H. (2003). Desempenho de sementes de milho em relação à sua localização na espiga. Ciênc Agrotec, 27 (4), 765-770.
Iamanaka, B.T., Taniwaki, M. H., & Oliveira, I. S. (2010). Micotoxinas em alimentos. Anais da Academia Pernambucana de Ciência Agronômica, (7), 138-161.
Márcia, B.A., & Lazzari, F.A. (1998). Monitoramento de fungos em milho em grão, grits e fubá. Ciência Tecnologia Alimentos,18(4),363-7.
Machinski, M.Jr., Valente-Soares, L. M., Sawazaki, E., Bolonhezi, D., Castro, J.L., Bortolleto, N. (2001). Aflatoxins, ochratoxin A and zearalenone in Brazilian corn cultivars. J. Scien. Food Agricult, 81, 1001-1007. http://dx.doi.org/10.1002/jsfa.882
Marques, O.J., Vidigal-Filho, P.S., Dalpasquale, V.A., Scapim, C.A., Pricinotto, L.F., & Machinski M. (2009). Incidência fúngica e contaminações por micotoxinas em grãos de híbridos comerciais de milho em função da umidade de colheita. Act Scient Agro,31(4), 667- 75. http://dx.doi.org/10.4025/actasciagron.v31i4.5690
Ministério da Saúde. Resolução RDC No.7. (2011). Dispõe sobre limites máximos tolerados (LMT) para micotoxinas em alimentos. Diário Oficial da União. Brasília, DF, 9 mar. 2011. Seção I, p. 66.
Oliveira, M.S., Prado, G., Abrantes, F.M., Santos, L.G,, & Veloso, T. (2002). Incidência de aflatoxinas, desoxinivalenol e zearalenona em produtos comercializados em cidades do estado de Minas Gerais no período de 1998 - 2000. Rev Inst Adolfo Lutz, 61(1), 1-6.
Pereira, M.L.G., Carvalho, E.P., & Prado, G. (2002). Crescimento e produção de aflatoxinas por Aspergillus flavus e Aspergillus parasiticus.B. Ceppa. 20 (1), 141- 156.
Pezzini, V. et al. Incidência de fungos e micotoxinas em grãos de milho armazenados sob diferentes condições. Rev Inst Adolfo Lutz, 64(1):91-6, 2005.
Ramos C.R.B.A, Brasil E.M, Geraldine R.M. (2008). Contaminação por aflatoxinas em híbridos de milho cultivados em três regiões do estado de Goiás. Pesquisa Agropecuária Tropica, 38(2), 95-102.
Santin, J. A., Reis, E. M., Matsumura, A. T. S., & Moraes, M. G. (2004). Efeito do retardamento da colheita de milho na incidência de grãos ardidos e de fungos patogênicos. Revista Brasileira de Milho e Sorgo, 3 (2), 182-192.
Soares, L.M., & Rodriguez-Amaya, D.B. (1989). Survey of aflatoxins, achratoxin A, zearalenone and sterigmatocystin in brasilian foods by using multitoxin layer chromatographic methods. J Assoc Anal Chem, 73, 22-6.
Villa-Martínez, A., Pérez-Leal, R., Morales-Morales, H.A., Basurto-Sotelo, M., Soto-Parra, J.M., & MartínezEscudero, E. (2015) Situación actual en el control de Fusarium spp. y evaluación de la actividad antifúngica de extractos vegetales Acta Agron, 2015, 64 (2), 194- 205.
Visconti, A., & Pascale, M. (1998). Determination of zearalenone in corn by means of immnoaffinity cleanup and high-performance liquid chromatography with fluorescence detection. J Chromatogr, 815(1), 133-40.